Das Bohrsche Atommodell, entwickelt von Niels Bohr im Jahr 1913, stellt einen fundamentalen Meilenstein in der Quantenphysik dar. Es beschreibt die Struktur des Atoms und die Bewegungen der Elektronen in klar definierten Bahnen um den Atomkern. Dieses Modell ist nicht nur für die Grundlagenforschung von Bedeutung, sondern spielt auch eine entscheidende Rolle in der Photovoltaik, insbesondere im Verständnis des Energieaustausches zwischen Licht und Materie.
Grundzustand und angeregte Zustände
Im Bohrschen Atommodell bewegen sich Elektronen auf bestimmten, diskreten Energieniveaus (auch Orbitale genannt) um den Atomkern. Der niedrigste Energiezustand eines Elektrons wird als Grundzustand bezeichnet. Solange dem System keine zusätzliche Energie zugeführt wird, verbleibt das Elektron in diesem stabilen Zustand.
Video 1: Schematische Darstellung des Atommodells nach Bohr
Sobald jedoch Energie in Form eines Photons absorbiert wird, kann ein Elektron in einen höheren Energiezustand springen. Dieses Prinzip ist für die Photovoltaik von zentraler Bedeutung, da Solarzellen genau diesen Mechanismus nutzen, um Lichtenergie in elektrische Energie umzuwandeln.
Energiezufügung durch Photonen
Die Energie eines Photons ist quantisiert und folgt der Gleichung:
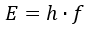
wobei E die Energie des Photons, h das Plancksche Wirkungsquantum und f die Frequenz des Lichts ist. Trifft ein Photon mit einer passenden Energie auf ein Elektron im Grundzustand, wird dieses auf ein höheres Energieniveau angehoben. Diese quantisierten Energiezustände sind ein Kernelement des Bohrschen Modells und erklären, warum nur bestimmte Photonenenergien absorbiert werden können.
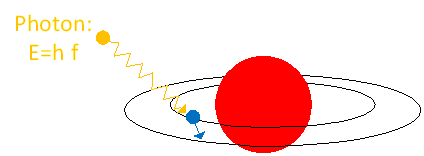
Abbildung 2: Niveauanhebung eines Elektrons (Photoeffekt)
Dieses Konzept ist essenziell für die Funktionsweise von Solarzellen: Die Materialien in der Solarzelle sind so ausgelegt, dass sie Photonen bestimmter Wellenlängen effizient absorbieren und so den Photostrom generieren können.
Energieniveaus und Orbitale
Im Bohrschen Modell sind die Elektronenbahnen nicht beliebig, sondern durch diskrete Energieniveaus festgelegt. Die Energieniveaus werden mit der Hauptquantenzahl n beschrieben, wobei n = 1 dem Grundzustand entspricht, n = 2, 3, 4 usw. angeregte Zustände darstellen. Die Energiedifferenz zwischen zwei Niveaus bestimmt die Energie des absorbierten oder emittierten Photons:
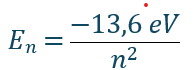
Diese quantisierten Energieniveaus sind von fundamentaler Bedeutung für die Absorption und Emission von Licht in Halbleitermaterialien, die in Solarzellen verwendet werden. Durch das Verständnis dieser Prozesse können Materialien gezielt so entwickelt werden, dass sie das Sonnenlicht optimal nutzen und die Energieausbeute maximieren.
Festkörper und ihre physikalischen Eigenschaften
Die Festkörperphysik ist entscheidend für das Verständnis der Photovoltaik, da Solarzellen aus speziellen Festkörpermaterialien bestehen.
Gitterstruktur
Festkörper besitzen eine regelmäßige Gitterstruktur, in der Atome oder Ionen durch chemische Bindungen miteinander verbunden sind. Diese Struktur bestimmt maßgeblich die elektrischen Eigenschaften des Materials, da sie den Bewegungsraum der Elektronen beeinflusst.
Überlappung der Orbitale
In Festkörpern überlappen sich die Orbitale der benachbarten Atome, wodurch Elektronen nicht mehr nur einem einzelnen Atom zugeordnet sind. Stattdessen bilden sie gemeinsame Aufenthaltsbereiche, die das Auftreten von Energiebändern ermöglichen.
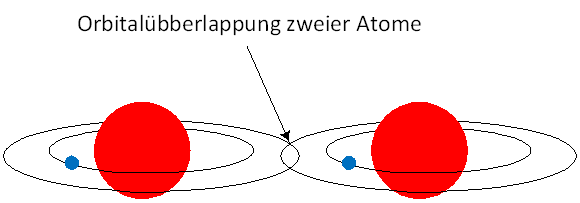
Abbildung 3 Orbitalüberlappung zweier Atome
Energiebänder und Bandlücken
Die Kombination vieler überlappender Orbitale führt zur Ausbildung von Energiebändern, bestehend aus:
- dem Valenzband, das mit Elektronen gefüllt ist,
- dem Leitungsband, in das Elektronen bei ausreichender Energieanregung übertreten können.
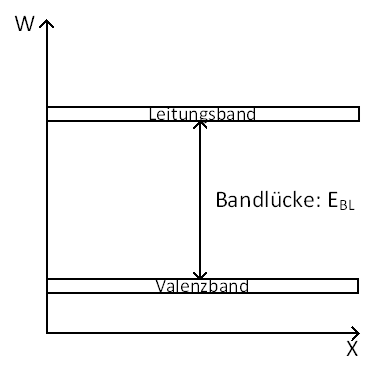
Abbildung 4: Schematische Darstellung Energiebänder
Zwischen diesen Bändern liegt die Bandlücke, die bestimmt, ob ein Material ein Leiter, Halbleiter oder Isolator ist:
- Leiter: keine oder sehr kleine Bandlücke,
- Halbleiter: moderate Bandlücke (~0,5 bis 3 eV),
- Isolatoren: große Bandlücke (> 3 eV).
Freie Elektronenbewegung und Stromfluss
Elektronen im Leitungsband können sich frei bewegen und tragen so zum elektrischen Stromfluss bei. In Halbleitern kann dieser durch Licht oder Spannung gezielt beeinflusst werden.
Bandanhebung durch Licht
Durch Absorption eines Photons kann ein Elektron vom Valenzband ins Leitungsband übergehen (Bandanhebung). Dieser Mechanismus ist zentral für die Photovoltaik, da er zur Entstehung freier Ladungsträger führt, die einen Strom erzeugen können.
Bedeutung für die Photovoltaik
Die Photovoltaik basiert auf der Umwandlung von Licht in elektrische Energie durch den photoelektrischen Effekt. Das Bohrsche Atommodell liefert die physikalische Grundlage für das Verständnis dieses Effekts: Elektronen werden durch Photonen angeregt, springen auf ein höheres Energieniveau und können durch ein elektrisches Feld in der Solarzelle zur Stromerzeugung genutzt werden.
Durch das gezielte Engineering von Halbleitermaterialien, wie Silizium oder Perowskiten, kann die Absorption von Photonen optimiert und der Wirkungsgrad von Solarzellen verbessert werden. Ein tiefgehendes Verständnis des Bohrschen Atommodells und der Festkörperphysik ermöglicht es, innovative Konzepte in der Photovoltaik weiterzuentwickeln und die Energiegewinnung aus Sonnenlicht effizienter zu gestalten.
